Что делать при отсутствии яйцеклетки в фолликуле
Овуляция, как известно – процесс перехода яйцеклетки из яичника в брюшную полость. Происходит она в результате разрыва фолликула. Однако в последнее время все чаще встречаются случаи, когда в фолликуле нет яйцеклетки.
Отсутствие яйцеклеток в фолликуле – серьезный недуг, не позволяющий женщине забеременеть. Сегодня он очень распространен – данная патология, если верить эпидемиологическим исследованиям, обнаружена у 5% женщин со всего мира. Причин, из-за которых женщина может столкнуться с этой проблемой достаточно много, вот самые серьезные из них:
Преждевременная менопауза. Обычный возраст прекращения менструаций – 45-55 лет. Наступление периода менопаузы рано или поздно предстоит каждой женщине. Однако, бывают случаи, когда этот процесс начинается значительно раньше, чем положено природой (обычно на 10-15 лет). С наступлением менопаузы (неважно, преждевременная она или нет, искусственная или естественная) женщина теряет естественную возможность рождения детей. Лечение преждевременной менопаузы возможно лекарственными препаратами, которые содержат эстроген. Не стоит принимать их самостоятельно – они канцерогенны, в результате их нерационального приема велика вероятность развития онкологических заболеваний.
Удаление яичников в результате хирургического вмешательства. Иногда врачам приходится прибегать к столь крайним мерам, чаще всего, это происходит в результате развития онкологических заболеваний. После того, как яичники удалены, естественная беременность у женщины уже невозможна. Шанс родить ребенка, в такой ситуации, женщине может дать только искусственное оплодотворение, т.е. донорская яйцеклетка.
Нет яйцеклеток: что делать?
В первую очередь, нужно обратиться к врачу, для выявления точней причины патологии, и наиболее подходящего метода терапии. Когда у женщины нет яйцеклеток, очень часто ей назначают гормональные препараты для стимуляции. Ни в коем случае нельзя принимать гормональные препараты самостоятельно – нерациональный прием препаратов эстрогена (как и любых других гормонов) может привести к самым непредсказуемым последствиям.
Если женщина, у которой в фолликуле отсутствует яйцеклетка, желает забеременеть, очень разумное решение вопроса – экстракорпоральное оплодотворение.
Народные средства, когда нет яйцеклеток
Процесс овуляции, и как следствие, появления яйцеклеток в фолликуле можно простимулировать народными средствами. Травы, положительно влияющие на стимуляцию овуляции – шалфей, подорожник и алоэ. Обычно их применяют в виде отваров. Приготовление отваров – процесс несложный. Обычно такая процедура проводится следующим образом: 1-2 ложки травы заливают одним стаканом воды, после чего полученную смесь доводят до кипения, а жидкость сливают.
Еще одно очень эффективное народное средство – эфирные масла. Для выработки эстрогена яичниками, который может благотворно влиять на рождение яйцеклеток, рекомендуется вдыхать пары масел шалфея, базилики, кипариса и аниса.
Специальная диета также необходима при отсутствии яйцеклеток. Потребление цитрусовых, ананасов, груш, капусты, инжира и риса женщинам следует сократить, а лучше, полностью убрать. Бобовые, помидоры, огурцы, гранаты, а также яблоки, наоборот, помогают процессу овуляции.
Повлиять на появление яйцеклеток может и витаминная терапия. Врачи, например, назначают фолиевую кислоту при недостаточной активности яичников.
Обратите внимание: лечение данной патологии только лишь народными средствами невозможно. Без консультаций специалиста женщинам, столкнувшимся с этой проблемой, решить ее будет очень сложно.
Российский центр доноров ооцитов предлагает широкий выбор доноров яйцеклеток для женщин, которые страдают различными патологиями репродуктивной системы. Обращайтесь к нам — и мы обязательно вам поможем!
www.oocyte.org
Синдром пустых фолликулов
Синдром пустых фолликуловВведение
Синдром пустых фолликулов (СПФ) впервые был описан Coulam и др. в 1986 г. Этот синдром представляет собой состояние, при котором, после адекватного ответа яичников на стимуляцию, при тщательной аспирации фолликулов не удается получить ооциты. СПФ при наличии доминантного фолликула встречается редко: всего у 0,045 (3,5%) пациенток, при пункции яичников (ПЯ) (Ben-Shlomo et al., 1991; Awonuga et al., 1998; Driscoll et al., 1998; Zreik et al., 2000; Aktas et al., 2005; Coskun et al., 2010; Mesen et al., 2011; Castillo et al., 2012).
Различают истинный (ИСПФ) и ложный (ЛСПФ) СПФ. ИСПФ определяют как невозможность получения ооцитов из зрелых яичниковых фолликулов после индукции овуляции при нормальном их развитии и нормальном стероидогенезе на фоне оптимального уровня β-ХГЧ в день аспирации. О ЛСПФ говорят в тех случаях, когда ооциты не удается получить на фоне низкого уровня β-ХГЧ из-за ошибок его введения или низкой биологической активности (Stevenson and Lashen, 2008).
Механизм возникновения ИСПФ остается неясным. Некоторые авторы даже сомневаются в самом существовании этого синдрома (Ben-Shlomo et al., 1991; Harrison and Fawzy, 1996).
Приводим описание случая, в котором у пациентки при четырех ПЯ не удавалось получить ооциты. Еще в трех циклах при аспирации было получено всего от одного до четырех ооцитов низкого качества. Изменение протокола лечения привело к успеху.
Пациенты и методы
Клинический случай
На консультацию обратилась супружеская пара по поводу 25-месячного первичного бесплодия. Женщина 24 лет отмечала нерегулярные менструации, начиная с менархе в 12-летнем возрасте при максимальной длительности аменореи 50 дней. Ее ИМТ составлял 26 кг/м2. При физикальном обследовании не было обнаружено ни угревой сыпи, ни гирсутизма. УЗИ тазовых органов патологии не выявило; эндометрий имел нормальную толщину 8 мм, размер фолликула – 20 мм. Гормональный профиль в ранней фолликулярной фазе был нормальным; уровень ФСГ составлял 4,89 МЕ/л. Ранее отмечалось некоторое повышение уровня пролактина, а при компьютерной томографии гипофиза было выявлено образование в 6 мм, что позволяло предполагать микроаденому. Однако пациентка не получала антидофаминергических средств, и все последующие анализы обнаруживали нормальный уровень пролактина. Гистеросальпингография – без изменений.
Муж пациентки, 28-летний водитель грузовика, выкуривал 30 сигарет в сутки. При физикальном обследовании у него обнаружено варикоцеле третьей степени. При анализе эякулята – олигоастенозооспермия (13 млн/мл, подвижных сперматозоидов 40%). Впоследствии ему была произведена субингвинальная перевязка сперматической вены.
Спонтанная беременность не наступала, и через 9 месяцев супружеская пара вновь обратилась в клинику. Была проведена индукция овуляции кломифеном цитратом (два цикла) или гонадотропинами (два цикла) с внутриматочной инсеминацией (ВМИ). Несмотря на нормальный ответ яичников и введение в матку 3–10 млн подвижных сперматозоидов в каждом цикле, беременность не наступила. С 2005 по 2011 гг. восемь раз использовали вспомогательные репродуктивные технологии (ВРТ) (табл. 1). Судя по уровню эстрадиола (Е2) и результатам УЗИ, ответ яичников был адекватным, но в четырех циклах ооциты при аспирации получены не были. В одном из циклов (но не в других) высокие уровни прогестерона указывали на преждевременную лютеинизацию в качестве возможной причины отсутствия ооцитов. В двух случаях безуспешной аспирации уровни β-ХГЧ составляли 44 и 70 МЕ/л. Еще в трех циклах удавалось получать от одного до четырех ооцитов, только два из которых оказывались зрелыми, и их оплодотворяли in vitro. При этом не было получено эмбрионов, пригодных для переноса. При хромосомном анализе у пациентки обнаружен нормальный женский кариотип.
В последнем (успешном) цикле вводили агонисты ГнРГ (трипторелин ацетат, декапептил, 0,1 мг*2) за 40 ч до пункции яичников. Во избежание нежелательных клинических последствий беременности, наблюдаемых при использовании аналогичных протоколов, за 34 ч до ПЯ вводили рекомбинантный ХГЧ (хориогонадотропин альфа, овитрель, 250 мкг, Serono). При аспирации было получено 18 ооцитов, 16 из которых оказались зрелыми, и в них инъецировали сперматозоиды. Всего развилось 11 эмбрионов; 2 были перенесены в матку, а 9 заморожены. В день переноса эмбрионов начинали поддержку лютеиновой фазы прогестероном и Е2. Наступила одноплодная беременность и через 38 недель женщина родила здорового мальчика весом 2600 г.
Обсуждение
СПФ – редкое, сложное и тревожное для пациентов состояние, при котором после стимуляции яичников, несмотря на явно нормальное развитие фолликулов и нормальный уровень Е2, не удается получить ооциты. Различают «истинный» СПФ, когда уровень ХГЧ в день получения ооцитов оптимален, и «ложный» СПФ, когда уровень ХГЧ снижен (Stevenson and Lashen, 2008). Однако относительно оптимального уровня ХГЧ существуют разногласия.
По данным Aktas et al. (2005), в день ПЯ уровень ХГЧ при правильном его введении колеблется в пределах 98–161 МЕ/л. Driscoll et al. (2000) нашли, что медиана концентрации ХГЧ в сыворотке после п/к введения 250 мкг рекомбинантного ХГЧ составляет 117,1 МЕ/л (колебания: 48–249 МЕ/л), а после в/м введения 5000 МЕ мочевого ХГЧ – 83,6 МЕ/л (колебания: 32–99 МЕ/л). Stevenson and Lashen (2008) на основании обширного обзора данных заключили, что за границу между нормальным и низким уровнем ХГЧ в день ПЯ следует принимать 40 мМЕ/мл. Ndukwe et al. (1996), пытаясь выявить предикторы СПФ, нашли, что во всех случаях СПФ уровень ХГЧ в сыворотке составлял < 10 мМЕ/мл.
Предполагается также существование пограничной формы СПФ, при которой из нескольких зрелых фолликулов удается получить очень мало зрелых или незрелых ооцитов (Is¸ik and Vicdan, 2000; Nikolettos et al., 2004; Duru et al., 2007; Desai et al., 2009; Vutyavanich et al., 2010).
Частота
Согласно найденным данным, частота СПФ колеблется от 0,045% до 3,4% (табл. 3). Эти колебания могут объясняться разными критериями исключения. В одни исследования включались пациентки с плохой реакцией на индукцию овуляции или с преждевременной овуляцией, в другие – нет. Случаи рецидивирующего ИСПФ встречаются крайне редко. Именно поэтому в литературе отсутствуют описания серии случаев, а некоторые авторы вообще отрицают существование этого синдрома.
Механизм развития
Этиология ИСПФ неизвестна. После его первого описания ряд авторов высказывал сомнения в реальном существовании этого синдрома. Считается, что феномен СПФ может объясняться преждевременной овуляцией, плохим ответом яичников или недостаточностью ХГЧ (Awadalla et al., 1987; Ben-Shlomo et al., 1991; Asch et al., 1992; Greb et al., 1993; Aktas et al., 2005). Отсутствие ооцитов, несмотря на правильное введение ХГЧ, может быть следствием низкой биологической активности последнего, связанной с различиями его всасывания или клиренса (Zegers-Hochschild et al., 1995; Hirshfeld-Cytron and Kim, 2008), различиями пороговых уровней ХГЧ, вызывающих ответ фолликулов, различиями сроков, за которые ХГЧ индуцирует созревание комплекса ооцит/кумклюс (Vutyavanich et al., 2010) или разным качеством препаратов ХГЧ (Zegers-Hochschild et al., 1995). Гипотезу о низкой доступности ХГЧ для яичников как причине СПФ подтверждает случай одностороннего СПФ при перекруте яичника, возникшем между временем введения ХГЧ и аспирацией фолликулов. Ооциты пришлось аспирировать из сохранного яичника (Stefunidis et al., 2002). Предполагались и другие причины, включая старение яичников (Ben-Shlomo et al., 1991; Greb et al., 1993; Lorusso et al., 2005), дисфункциональный фолликулогенез, обусловленный активацией апоптоза и атрезией фолликулов (Desai et al., 2009), нарушение функции клеток гранулезы (Zreik et al., 2000), дефекты развития и созревания ооцитов (La Sala et al., 1991; Bustillo, 2004; Kourtis et al., 2004; Inan et al., 2006; Duru et al., 2007), прочное прикрепление комплексов кумклюс/яйцеклетка к стенкам фолликулов, нарушение индукции овуляции (Tsuiki et al., 1988; Khalaf et al., 2000), а также генетический дефект (Papier et al., 2000; Onalan et al., 2003; Vujisic et al., 2005; Yariz et al., 2011).
Tsuiki et al. (1988) обнаружили в фолликулярной жидкости пациентки с СПФ высокую концентрацию Е2 и андростендиона и низкий уровень прогестерона. О низком уровне прогестерона и высокой концентрации тестостерона сообщили также Phocas et al. (1992), хотя, по их данным, низким был и уровень Е2 (Tsuiki et al., 1988; Phocas et al., 1992). Возможно на поздней стадии фолликулогенеза происходит потеря ооцитов вследствие апоптоза. Недавно у двух сестер с ИСПФ была обнаружена новая мутация в гене рецептора ЛГ/ХГЧ (Yariz et al., 2011). Существование пограничных случаев СПФ позволяет предполагать нарушение процессов созревания ооцитов и экспансии клеток кумулюса.
Терапевтический подход
Лечение СПФ представляется трудной задачей. Универсального терапевтического подхода не существует. Некоторые авторы, исходя из низкой частоты рецидивных случаев, рекомендуют повторно использовать стандартные циклы ВРТ независимо от протокола лечения (Ben-Shlomo et al., 1991). Если в цикле с СПФ для десенситизации использовались агонисты ГнРГ, то в повторной попытке предлагается использовать антагонгисты (Krishna et al., 2008) и наоборот. В тех случаях, когда ооциты не удается аспирировать из одного яичника, а уровень ХГЧ низок, некоторые авторы предлагают повторно вводить ХГЧ из другой партии и пунктировать второй яичник (Khalaf and Braude, 1997; Ndukwe et al., 1997; Awonuga et al., 1998; Quintans et al., 1998; Evbuomwan et al., 1999; Esposito and Patrizio, 2000; Papier et al., 2000; Reichman et al., 2010) или даже производить повторную аспирацию тех же фолликулов (Meniru and Craft, 1997; Hassan et al., 1998; Snaifer et al., 2008). Другие предлагают заменять мочевой препарат ХГЧ на рекомбинантный (Penarrubia et al., 1999). Hourvitz et al. (2010) описал два случая СПФ, в которых удалось добиться созревания ооцитов in vitro.
Две особенности терапии описываемого случая, требующие специального рассмотрения, заключаются в применении агонистов ГнРГ для окончательного созревания ооцитов (Lok et al., 2003) и удлинении временного интервала между запуском овуляции и пункцией яичников (Uygur et al., 2003).
Агонист ГнРГ для индукции окончательного созревания ооцитов
В течение длительного времени для имитации выброса ЛГ используют ХГЧ. Позднее было показано, что запуск овуляции можно осуществить с помощью агонистов ГнРГ (Shalev et al., 1994; Fauser et al., 2002; Griesinger et al., 2006). К возможным преимуществам применения агонистов ГнРГ для окончательного созревания ооцитов относится одновременная индукция выброса ФСГ (Gonen et al., 1990; Fauser et al., 2002). Роль выброса ФСГ в середине цикла не совсем ясна. Имеются данные, что ФСГ индуцирует появление рецепторов ЛГ на лютеинизирующихся клетках гранулезы, способствуя созреванию ядерных ооцитов и экспансии кумулюса (Byskov et al., 1997; Humaidan et al., 2011). ФСГ также удерживает открытыми щелевые контакты между ооцитом и клетками кумулюса, играя тем самым важную роль в проведении сигналов (Godard et al., 2009; Lamb et al., 2011). ФСГ повышает активность активатора плазминогена в клетках гранулезы, что приводит к образованию плазмина в фолликулярной жидкости (Strickland and Beers, 1976). Плазмин, в свою очередь, активирует коллагеназу, разрушающую стенку фолликула (D’Alessandris et al., 2001; Lamb et al., 2011). Экспансия и дисперсия клеток кумулюса позволяет клеточной массе ооцит/кумулюс перед овуляцией отъединиться от стенки фолликула. Этот процесс включает стимулируемый ФСГ синтез матриксной гиалуроновой кислоты (Dell’Aquila et al., 2004). Введение ФСГ вместе с триггером овуляции (ХГЧ) увеличивает число получаемых ооцитов и улучшает оплодотворение (Lamb et al., 2011). Рецепторы ГнРГ обнаружены во многих тканях человека, включая преовуляторные клетки гранулезы. У млекопитающих от рождения и до выброса гонадотропинов в пубертате ооциты остаются в профазе первого мейоза. В течение этого длительного времени внутриклеточные цАМФ и цГМФ препятствуют возобновлению мейоза ооцитов. ЛГ снижает уровень цГМФ, и мейоз возобновляется (Sun et al., 2009). Показано, что активация периферических рецепторов ГнРГ снижает уровень цАМФ в клетках. ГнРГ индуцирует транскрипцию нескольких генов, участвующих в процессах разрыва фолликулов и созревания ооцитов (Yu et al., 2011). Положительные результаты восьмого цикла лечения у данной пациентки могут объясняться выбросом ФСГ и непосредственным действием агонистов на рецепторы ГнРГ в яичниках. Можно предположить, что по какой-то неизвестной причине механизм действия ЛГ у пациентки оказался заблокированным, а агонисты ГнРГ активировали иной механизм.
Удлинение интервала между запуском овуляции и пункцией яичников
В естественных циклах выброс ЛГ начинается за 34–36 ч до разрыва фолликулов (Yu et al., 2011). Подобно этому, введение экзогенного ХГЧ вызывает разрыв фолликулов примерно через 37 ч (Edwards and Steptoe, 1975). Мейоз возобновляется через 18 ч после начала выброса ЛГ (Seibel et al., 1982). Для максимального созревания ооцитов концентрация ЛГ должна оставаться выше пороговой в течение 14–27 ч (Zelinski-Wooten et al., 1992). Разрыв фолликулов и созревание ооцитов – процессы, разворачивающиеся во времени, причем у разных женщин это время различно. Можно предположить, что экспансия кумулюса, обусловливающая отсоединение ооцита от стенки фолликула, у некоторых женщин также требует большего времени. В таких случаях, если аспирацию производят через 34 ч после введения ХГЧ, может наблюдаться СПФ.
Заключение
Описанный случай доказывает существование ИСПФ. Пациентку явно нельзя было отнести к группе недостаточно реагирующих на стимуляцию яичников, так как после стимуляции у нее постоянно регистрировался повышенный уровень Е2, а УЗИ обнаруживало множество фолликулов. ХГЧ она получала в нужной дозе, о чем свидетельствует его концентрация в сыворотке. Мы не можем исключить нарушения всасывания или клиренса ХГЧ в качестве причины несколько сниженного его уровня у нашей пациентки в сыворотке, но, поскольку этот уровень все же превышал регистрируемый в других случаях СПФ, полагаем, что следует искать другую причину.
В завершившемся успехом цикле комбинировались два подхода: для окончательного созревания ооцитов использовались агонисты ГнРГ и было удлинено время между запуском овуляции и ПЯ. Невозможно решить, какой из этих факторов обусловил желаемый результат. Скорее всего, основную роль сыграло не добавление ХГЧ за 34 ч до ПЯ, поскольку раньше многократное использование такого режима не приводило к успеху. Однако желаемый исход мог быть обусловлен сочетанием ХГЧ с агонистами ГнРГ. Нельзя исключить и того, что положительный результат каким-то образом связан со временем (29 мес.), прошедшим между предыдущими попытками получения ооцитов и успешным циклом. Иными словами, СПФ может быть самоизлечивающимся состоянием.
Мы настаиваем на существовании ИСПФ, доказывая это описанным случаем. В то же время, мы считаем СПФ неточным термином, поскольку на самом деле фолликулы не пусты. По-видимому, с помощью стандартных методов ВРТ их просто не удается аспирировать или найти. СПФ может быть следствием нарушения функции клеток гранулезы, при котором не возобновляется мейотическое созревание ооцитов, не происходит экспансии кумулюса, а незрелые комплексы ооцит/кумулюс не поддаются аспирации. В описанном случае удлинение интервала между запуском овуляции и ПФ и использование для нндукции овуляции агонистов ГнРГ обусловили возможность аспирации зрелых ооцитов и завершившуюся родами беременность. Причины неудач обычного режима ЭКО и успеха нового подхода в данном случае остаются неясными.
R. Beck-Fruchter, A. Weiss, M. Lave, Y. Geslevich и E. Shalev
reproductologist.com
каковы причины отсутствия и нарушения роста, а также поговорим о персистенции, спящих яичниках и кисте
Процесс фолликулогенеза с последующей овуляцией – неотъемлемая часть гормональных изменений женщины репродуктивного возраста. В гинекологической практике существует множество ситуаций, когда доминантный фолликул созревает, а овуляция так и не происходит.
Если говорить более просто, то «граафов пузырек» просто не лопается, а продолжает прогрессировать или оставаться в неизменном состоянии. Подобная клиническая картина является патологией, у которой есть свои причины возникновения. В таком случае врач должен провести детальную диагностику пациентки, чтобы разработать план лечения и выяснить этимологию заболевания.
Этапы развития
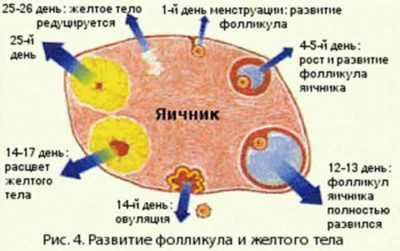 Фолликул – это небольшая капсула, которая располагается на левом и правом яичнике. С момента первой отслойки эндометрия (месячные) фолликулы начинают прогрессировать в размерах. Это физиологическая норма, которая говорит в пользу репродуктивного здоровья женщины.
Фолликул – это небольшая капсула, которая располагается на левом и правом яичнике. С момента первой отслойки эндометрия (месячные) фолликулы начинают прогрессировать в размерах. Это физиологическая норма, которая говорит в пользу репродуктивного здоровья женщины.Именно по этой причине первая фаза менструального цикла называется «фолликулярной», так как именно в первые 11-16 дней активизируется процесс фолликулогенеза. После овуляции капсулы естественным образом отмирают, регрессируют, а доминантный фолликул вообще исчезает, превращаясь в желтое тело.
Тем не менее процесс роста фолликула в первую фазу можно наглядно представить таблицей. Стоит помнить, что это только среднестатистические цифры, которые актуальны для менструального цикла в 28 дней. Если он короче или длиннее, то размеры фолликулов будут распределяться немного иначе.
| День менструального цикла | Размер фолликула |
| 1-4 | 1-3 мм |
| 5 | 5-6 мм |
| 6 | 6-7 мм |
| 7 | 7-8 мм |
| 8 | 9 мм |
| 9 | 10-12 мм |
| 10 | 12-14 мм |
| 11 | 14-16 мм |
| 12 | 16-18 мм |
| 13 | 18-20 мм |
| 14 (день овуляции) | 20-22 мм |
«Граафов пузырек» увеличивается в диаметре с каждым днем на 1-2 мм, что обусловлено гормональной активностью. На 11-16 день он переполняется жидкостью и фиксируется на УЗИ в размерах от 18 до 22 мм. При подобном диаметре капсула в идеале разрывается, но такой циклический процесс происходит не всегда. В случае патологий фолликулы могут созревать неправильно, а это в свою очередь блокирует овуляцию.
СПРАВКА! Быстрее всех остальных капсул развивается именно доминантный фолликул или «граафов пузырек», в котором зреет яйцеклетка (ооцит). Все остальные клетки не превышают в размерах 8 мм. После овуляции они регрессируют или полностью исчезают.Причины отсутствия овуляции
 Если «граафов пузырек» не лопнул, то овуляция невозможна. Такая клиническая картина является следствием патологических процессов, среди которых выделяют следующие состояния и диагнозы:
Если «граафов пузырек» не лопнул, то овуляция невозможна. Такая клиническая картина является следствием патологических процессов, среди которых выделяют следующие состояния и диагнозы:- Фолликулярная киста.
- Персистенция.
- Лютеинизация.
- Гиперпролактенемия.
- Дисфункция яичников гормонального генеза.
- Заболевания гипофиза, гипоталамуса.
- Нарушения работы щитовидной железы.
- Стресс.
- Голодание.
- Прием КОК.
Причину ановуляции должен устанавливать только врач, назначая необходимые анализы и диагностические процедуры (УЗИ). Самостоятельно и «на глаз» лечение не назначается, так как каждый клинический случай индивидуален.
Последствия
Последствия ановуляции и не исчезающего фолликула напрямую зависят от причины, повлекшей такие патологические изменения. Если всему виною стресс и голодание, то организм достаточно быстро восстанавливается после устранения провоцирующих факторов.
В остальных случаях последствия могут разные:
- Рост фолликулярной кисты.
- Разрыв кистозного образования (перитонит).
- Появление доброкачественных или злокачественных опухолей.
- Дисфункция яичников.
- Прогрессирование патологий гипофиза, гипоталамуса.
- Бесплодие.
- Развитие гинекологических заболеваний (эндометриоз, поликистоз).
Подобный исход возможен только в том случае, если пациентка пренебрегает лечением и не обращается к врачу.
СПРАВКА! Фолликулярная киста размером до 45 мм в большинстве случаев рассасывается сама без дополнительного лечения спустя 3-4 месяца.
Персистенция
 В гинекологии персистенцией называют состояние, когда доминантный фолликул постоянно фиксируется на датчиках УЗИ в независимости от фазы менструального цикла. При этом овуляция отсутствует, как и само желтое тело.
В гинекологии персистенцией называют состояние, когда доминантный фолликул постоянно фиксируется на датчиках УЗИ в независимости от фазы менструального цикла. При этом овуляция отсутствует, как и само желтое тело.От кисты такая клиническая картина отличается тем, у персистирующего фолликула вполне нормальные для овулирования размеры (до 24 мм).
При персистенции «граафова пузырька» у пациенток концентрируется в крови слишком много эстрогена, а также фолликулостимулирующего гормона (ФСГ). Прогестерона и лютеина при этом совсем мало или недостаточно для того, чтобы наступила овуляция.
При таком состоянии женщина может испытывать определенные клинические симптомы:
- Задержка менструации.
- Невозможность забеременеть.
- Отсутствие овуляции долгое время.
В большинстве случаев пациентки отмечают только небольшую задержку месячных. В основном, персистирующий фолликул обнаруживается случайно во время профилактического прохождения УЗИ.
ВАЖНО! Несмотря на то, что персистенция фолликула отлично поддается лечению, существует немалая вероятность, что «граафов пузырек» в дальнейшем трансформируется в кистозное образование. Лечение и наблюдение в таком случае обязательно.
Спящие яичники
 Понятие «спящие яичники» не существует официально в медицинской практике. Под этим обычно понимается «дисфункция яичников», которая означает органические или эндокринные нарушения репродуктивной системы.
Понятие «спящие яичники» не существует официально в медицинской практике. Под этим обычно понимается «дисфункция яичников», которая означает органические или эндокринные нарушения репродуктивной системы.Внешне это выражается в удлинении менструального цикла (задержка больше 35 дней) или его укорочении (меньше 21 дня). Такое состояние может быть вызвано только двумя причинами:
- Органические, то есть различные заболевания (эндометриоз, поликистоз, киста, аденома гипофиза), которые отрицательно влияют на процесс фоллликулогенеза, овуляции.
- Эндокринные, то есть переизбыток или недостаток некоторых гормонов.
Только после осуществления диагностических мероприятий (кольпоскопия, УЗИ, анализы крови на половые гормоны) можно назначать лечение. При «спящих яичниках» практически невозможно забеременеть поэтому такой диагноз является частой причиной бесплодия.
СПРАВКА! Дисфункция яичников иногда является симптомом раннего климакса, а также клиническим признаком надвигающейся менопаузы, если возраст женщины более 45 лет.
Нарушение роста
 Усиленный рост фолликулов отмечается в 1 фазу цикла, а после разрыва наблюдается их закономерный регресс. Это значит, что созревание капсул начинается с 1 дня менструации.
Усиленный рост фолликулов отмечается в 1 фазу цикла, а после разрыва наблюдается их закономерный регресс. Это значит, что созревание капсул начинается с 1 дня менструации.Если в организме имеются гормональные или органические нарушения, то процесс фолликулогенеза будет происходить с заметными нарушениями. У пациентки в таком случае будет наблюдаться:
- Аменорея (отсутствие менструации)
- Ановуляция
- Дисфункция яичников.
- Задержка менструации.
- Нерегулярный менструальный цикл.
Все эти состояния являются распространенной причиной бесплодия, так как менструальный цикл проходит с патологиями. У женщины может проявляться разная клиническая картина:
- Фолликул не созревает до максимальных размеров и быстро регрессирует.
- «Граафов пузырек» не разрывается и остается в неизменном состоянии (персистенция), либо трансформируется в кисту.
- Яйцеклетка не созревает и не выходит в фаллопиевы трубы, овуляция не происходит, но «граафов пузырёк» начинает секретировать прогестерон (лютеинизация).
Подобная патология прогрессирует вследствие генетических, эндокринных и органических нарушений. Чаще всего причина кроется в гормональном дисбалансе, который происходит в фолликулярную фазу цикла (дефицит или переизбыток ФСГ, эстрогена, пролактина).
Киста яичника
 Во многих случаях причиной ановуляции является кистозное образование, которое формируется из неовулировавшего фолликула.
Во многих случаях причиной ановуляции является кистозное образование, которое формируется из неовулировавшего фолликула.Врач подозревает подобное новообразование только в том случае, если «граафов пузырек» превышает 25 мм в диаметре. В остальных случаях это будет персистенция или лютеинизация капсулы.
Кисту реально определить только по результатам УЗИ, так как при кольпоскопии и обычном гинекологическом осмотре это сделать невозможно. Она фиксируется на мониторах как анэхогенное округлое образование с ровными контурами и однородным жидкостным содержимым.
Размеры кисты при этом играют решающее значение, так как от этого зависит дальнейший прогноз и лечение.
ВАЖНО! При небольших размерах кистозного новообразования (до 50 мм) лечение не требуется, так как через 1-4 месяца киста рассасывается самостоятельно, не причиняя вреда организму. При размерах более 60 мм необходимо гормональная терапия или в крайних случаях хирургическая лапараскопия.
Если киста превышает 80 мм в диаметре, то существует огромный риск ее разрыва с последующим перитонитом. Выжидательная позиция и лекарственная терапия в таком случае несет огромную опасность.
В заключение необходимо сказать, что созревание фолликула без последующей овуляции явление довольно-таки частое. При такой патологии невозможно зачатие, так как яйцеклетка остаётся внутри капсулы и не выходит к фаллопиевым трубам.
Прогестерон, необходимый для утолщения эндометрия, практически не секретируется. Если вовремя не обратиться к врачу и пустить все «на самотек», то существуют высокие риски осложнений и появления более опасных заболеваний.
mirmamy.net

Добавить комментарий